はじめに
テレビのニュースやワイドショーでは、連日のように新型コロナウイルスによる感染症COVID-19とその世界的流行(パンデミック)の経過について取り上げています。そして、今日(3月21日)のテレビ朝日のワイドショーでも紹介されていたのが「集団免疫による感染症流行の収束の可能性」です。
厚生労働省がCOVID-19対策の基本方針として、集団免疫理論に基づくように見える感染者数の推移の図を出して以来、テレビでは何度となく集団免疫という言葉が出てきています。このブログでもこの厚労省の図を紹介しながら、自然感染による集団免疫の非現実性について説いてきました(→手洗いと消毒ーウイルス除去の基本 )。
ここでは再度、COVID-19流行における集団免疫の意義を考え、それに大きな影響を及ぼすワクチン開発の状況について紹介したいと思います。
1. 集団免疫とワクチン
集団免疫については、このブログでも2年前に解説しました(→感染症と集団免疫)。これは、感染症においてその病原体の免疫を獲得した人が集団内に広がっていくと、それが同じ集団内の非免疫獲得者への防護効果となり、感染症拡大が抑制されるというものです。
図1にその考え方を示します。1人の感染者から5人の非感染者に伝染させるとすると(これを基本再生産数と言います)、集団免疫がない場合、それらの非感染者はすべて感染者になります(図1左)。一方、集団内にこの感染症に対する免疫獲得者が多数いると、それが防護壁になって感染者から非感染者(非免疫獲得者)に伝染しにくい状態になります(図1右)。
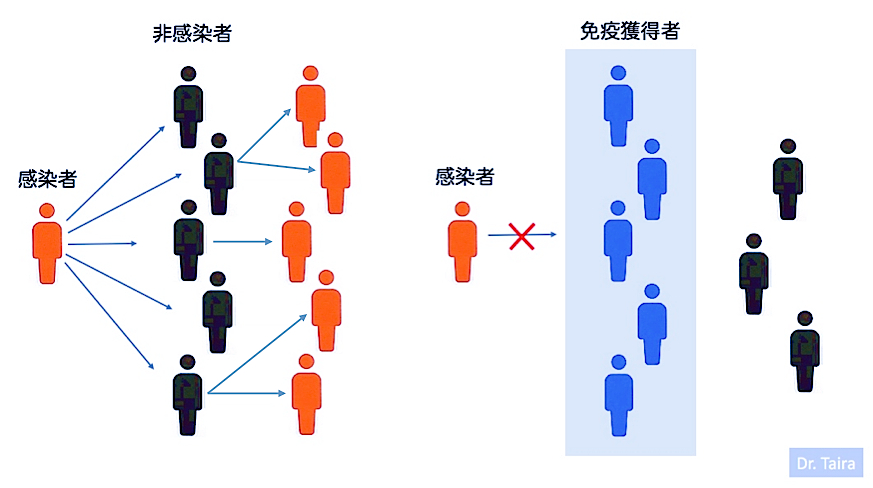 図1. 集団免疫理論による感染拡大の抑制効果.
図1. 集団免疫理論による感染拡大の抑制効果.
免疫を獲得する手段としては自然感染およびワクチン接種による人為的感染があります。いずれの場合においても、免疫獲得者が多ければ多いほど集団免疫の保護効果が高まります。
何割の人が免疫を獲得していれば集団免疫が有効になるかということ(集団免疫閾値)は、基本再生産数に依存します。図1の場合は基本再生産数=5ですので、集団免疫閾値=1–1/5=0.8となり、80%の人が免疫を獲得する必要があります。
今回のCOVID-19で考えると、基本再生産数=2.68と報告されていますので [1](範囲は2.5–2.9 [2])、仮にこの数字を基に考えると、同様な計算で63%の人が免疫を獲得していれば集団免疫の効果が現れるということになります。問題はここからです。テレビでは「集団免疫の効果」ばかりがクローズアップされていて、どうやって免疫を獲得するか、その免疫獲得のプロセスで何が起こるか、そもそも集団免疫理論が現実として可能かが、省略あるいは曖昧にされているのです。
国民の6割以上が免疫を獲得すれば感染症流行が収束するとあっさり言いますが、63%の自然感染で考えれば、日本では約8,000万人がウイルスに感染することになります。この数字に至るまで一体どのくらいの時間がかかるのでしょう。おそらく年単位の長期間になるはずで、その間の健康被害、経済的被害、社会的被害はとてつもなく大きくなることは容易に想像されます。
そして、仮にCOVID-19の致死率を1%とすると80万人が死亡する計算になります。この数字はとても国民が許容できる範囲のものではないでしょう。
このような自然感染による集団免疫で感染症拡大を抑制したという公式記録は、私が知る限りないように思われます。日本で38万人の犠牲者を出したスペイン風邪(インフルエンザ)のパンデミックでさえ、感染率4割と言われています。実際には獲得免疫だけではなく、自然免疫や物理的な隔離の機構も働くのではないでしょうか。
コロナウイルスに対する免疫は長続きしないという古い論文もあり、SARS-CoV-2についても獲得免疫が長期間持続するという保証もありません。このように、自然感染の集団免疫のみによる感染症抑制は、現実論としては受け入れられないのですが、テレビではゲストコメンテーターが出てきては実しやかに語られ、サラッと流れているという状況です。感染症流行が集団免疫で抑制できた例があれば是非教えてほしいものです。
英国では、ジョンソン首相による「多くの愛する人を失う」発言に続き、科学顧問が集団免疫理論を持ち出して「国民の6割が感染すればよい」と述べて批判されましたが [3]、むしろ当然のことだと思います。
要は、集団免疫を考える場合には、ワクチン接種(予防接種)による安全かつ持続的な免疫獲得を前提としなければ現実として意味をなさないということです。COVID-19に対するワクチンはまだありません。したがって、いかに早く安全かつ効果的なワクチンが開発され、実用化されるかが集団免疫に期待できるカギとして一般的には考えられています。
とはいえ、ワクチンでさえ、集団免疫に効くという保証はありません。集団免疫を働かせるためには免疫力の持続性と同調性が必要ですが、ワクチンの大規模接種のタイムラグと抗体価の経時的低下の可能性を考慮すると、集団内で免疫力にムラを生じやすくなり、免疫記憶されたとしても一定レベル以上に維持することは至難のワザです。つまり、国民の6–8割にほぼ同時期にワクチン接種すれば集団免疫力の同調性は維持されますが、これは現実的には不可能です。
厚労労働省は「新型コロナウイルスのワクチンの開発・使用開発はいつごろになりますか?」という問いに対して、現時点では以下のように答えています [4](以後更新される可能性あり)。
「ワクチンの開発は、ワクチンの有効性・安全性の確認や、一定の品質を担保しつつ、大量生産が可能かどうかの確認などを行う必要があります。一般に、ワクチンを開発し、使用可能となるまで、さまざまな工程がありますが、できるだけ早く開発できるよう支援に努めています」。
長々とした答えですが、具体的説明は何もなく、見通しは立っていないということを述べているようなものです。当該省が出した集団免疫理論に基づくと思われる「基本方針の図」に照らし合わせて、責任とより具体性をもって答えてほしいものです。それとも国民の6割が自然感染することを待っているのでしょうか。
あるいは、集団免疫理論に基づけば、強制隔離によって免疫獲得者と実質同じような状態を作れば、感染拡大が抑えられる可能性があります。つまり、少なくとも63%以上の人を隔離(たとえば都市封鎖)すれば、集団免疫と同様な効果が期待できるわけです。極論すれば、一定期間、100%「人と人」の接触を断てばこのパンデミックは抑えられます。
しかし、国はそのような接触削減の対策を今すぐに実施できるのでしょうか。少なくとも現段階では、国からそのような声は聞こえてきません。
2. 新型コロナウイルスの構造
新型コロナウイルスは正式にはSARS-CoV-2と呼ばれています。2002−2003年に流行した重症急性呼吸器症候群(SARS)の病原体であるコロナウイルスSARS-CoVによく似ているからです。
いま行われているCOVID-19対策としてのワクチン開発は、SARS-CoV-2の表面にあるタンパク質を抗原候補として、それを標的として行われています。そこでこのウイルスの形態と表面構造について簡単に説明したいと思います。
SARS-CoV-2は、ほかのコロナウイルス同様に、ウイルスの基本形であるカプシドがエンベロープという脂質膜に覆われた丸い構造をしています(図1)。カプシドの中には遺伝子としてのゲノム(1本鎖RNA)が入っています。エンベロープ表面にはスパイクと呼ばれる王冠状の突起が多数くっついており、コロナウイルスという名前の由来になっています。スパイクはSタンパクと呼ばれるタンパク質でできています。
ウイルスのスパイクがヒトの細胞の受容体 angiotensin-converting enzyme 2 (ACE2)に結合すると小胞に取り込まれ、スパイクを構成するSタンパクの解裂に続いてウイルス膜と細胞膜との融合が起こります。そして、細胞内にウイルスゲノム(RNA)が放出されます。このRNAはそのままmRNAとして働きタンパク質が合成され、ウイルスが再構成されます。
前に述べたように(→新型コロナウイルスは人為的改変体ではない )、SARS-CoV-2のスパイクタンパク質には、従来のコロナウイルスにはきわめて稀な塩基性アミノ酸解裂部位(polybasic cleavage site)が挿入されています。これによって、宿主タンパク分解酵素の作用で解裂しやすくなり、エンベロープ膜と宿主細胞膜との融合が起こりやすい(感染力が強い)と考えられています [5]。
3. スパイクタンパク質の解析と波及効果
米国テキサス大学オースティン校(University of Texas at Austin)のJ. マクレラン(J. S. McLellan)博士の研究室とNIAIDワクチン研究所の共同研究チームは、SARS-CoV-2のスパイクタンパク質の構造解析に関する論文を、2020年2月19日のサイエンス誌上に発表しました [6]。この研究成果はワクチンや治療法の開発に向けた重要な一歩と言えます。
研究チームは従来、SARSやMERSなどの感染症に関わるコロナウイルスを長年研究対象としてきた経験と実績があります。そのため、ウイルスタンパク質の分離、安定化、解析に関する技術基盤があり、彼らならではと感じる今回の迅速な研究成果の発表になりました。
もちろん、この前に中国チームによるSARS-CoV-2の全ゲノム解読の成果があり [7]、それがスパイクタンパク質の構造解析の必須情報として役立ったことは当然です。わずか2–3ヶ月で論文出版までこぎつける中国や米国の研究スピードには驚くばかりです。
以下このサイエンスの論文の内容を簡単にまとめてみましょう。
研究チームは、近縁コロナウイルスのゲノムの塩基配列との比較に基づいて、SARS-CoV-2のスパイクをコードすると推定される領域をクローン化・分離しました。そして培養細胞を用いてそのタンパク質を大量に発現させ、解析に用いました。
研究チームはスパイクタンパク質の構造解析にクライオ電子顕微鏡法を用いました。これは標的物の変性を避けるために超低温下で分子レベルでの構造を視る最新技術です。
得られた画像に基づいて、スパイクタンパク質の詳細な立体構造のイメージを作り上げました。そして、SARS-CoV-2のスパイクは従来のSARSウイルスのそれよりも10倍から20倍の強さでACE2に結合することを明らかにしました。これがこのウイルスの従来に見られない感染力の強さと人から人への伝播力の強さに繋がっているのです。
SARS-CoV-2とSARSウイルスは塩基配列や構造においては類似していますが、後者用に開発された3種類の抗体はいずれもがSARS-CoV-2のスパイクタンパクには反応しませんでした。この事実は、SARS-CoV-2に対するワクチンと抗体開発はまったく新しい戦略で取り組まないといけないことを示すものです。
現在、研究チームはSARS-CoV-2のスパイクタンパク質を標的とする抗体とワクチンの開発に取り組んでいます。このスパイクタンパク質を、COVID-19感染症から治癒した人たちに導入することで抗体を得る予定だと述べています。もしこの抗体が大量に生産可能となれば、スパイクタンパク質のワクチンとしての適用に先んじて、感染症の治療に使うことができるのです。
研究チームは、作成した分子構造の3D画像を世界各地の共同研究者らに送付するとしています。その目的は、このスパイクタンパク質が引き起こす免疫反応を増大させるなどの改良を促すことであり、世界の研究者の協力体制が強化されることでそれが可能になるでしょう。
4. mRNAワクチン
テキサス大学とNIAIDワクチン研究所の共同研究チームが合成・加工したスパイクタンパク質はワクチンの候補の一つであり、すでに臨床試験がなされています。一方で、抗原としてのタンパク質をワクチンとして使うのではなく、その元になっている核酸レベルでワクチン化するという試みが急速に進められています。
その中で、最も期待されているのがmRNAワクチンです。タンパク質は遺伝子の設計図であるDNAが写し取られた伝令RNA(メッセンジャーRNA、mRNA)の翻訳によって作られます。であるなら、タンパク質を用いるよりもその前のmRNAを用いた方が簡便性、応用性、コストの点でメリットがあるというわけです。
すなわち、mRNAを細胞に導入して細胞自身に抗原となるタンパク質を作らせれば、ワクチン生産のステップが簡略化でき、mRNAの塩基配列を変えるだけでタンパク質の構造を変えることが可能なので、応用性の面でも有利です。具体的には、たとえば筋肉注射でmRNAを含む微粒子を導入し、宿主細胞内でスパイクタンパク質を作らせるという方法です。
ただ、mRNAはそのままでは翻訳されないので末端を修飾する必要があり、抗原タンパク質の翻訳活性を保ったまま強い免疫賦活化作用を得る必要があります。そして、そもそも異物ですから、自然免疫機構を刺激して生体内で強い炎症反応(アジュバント効果)を引き起こす可能性があります。いわゆる副作用(side effects、日本ではなぜかワクチン用として副反応と呼称)の問題です。
治験の結果で用量が決まったとしても、mRNAの翻訳活性は個人差(年齢、性別、体格など)があると思われるので、非常に重篤な副作用をもたらす場合も予想されます。何よりもmRNAワクチンは前例がないものであり、健康体にスパイクコードmRNAを導入する未知の危険性もあるでしょう。
たとえば、抗体依存性免疫増強(ADE)はそのうちの一つです。重症急性呼吸器症候群(SARS)などの同じベータコロナウイルス感染症に対するワクチンの研究では、動物実験や培養細胞レベルでワクチン投与後のウイルス感染でADEの可能性が考えられています [8, 9]。そして、そもそもスパイクタンパク質自身に毒性はないことを、あらかじめ確かめておく必要があります。
mRNAワクチンの先駆的開発者であるK. カリコ博士は、人工mRNAに化学修飾を施しておくと(たとえば修飾ウリジンにすると)、mRNAを細胞内に導入しても安定して持続し、炎症反応が低く抑えられることを発見しています [10]。おそらくこのような工夫がなされることでしょう。しかし、これは必要以上にmRNAが体内に残ってしまうかもしれないという諸刃の剣的な処置です。
生体内の細胞に直接mRNAを送り込むことは容易ではなく、その導入方法の開発が重要となります。そのための加工技術(mRNAの包埋方法など)と大量発現の工夫、大量生産の方法の開発、経済性、そして免疫原性を評価など、クリアしなければならないいくつかの課題があります。
mRNAワクチンの欠点の一つはその安定性です。生体内にはRNAを分解する酵素があるので、外から侵入したRNAはすぐに分解されてしまいます。すぐに分解されることは安全性の面からは有利ですが、効果を発揮する前に消えてしまうのでは意味がありません。mRNAワクチンの開発に成功したとしても、それを包み込む媒体の開発(脂質ナノ粒子など)や実際には低温(−20〜−80℃)管理のサプライチェーンがないと普及はむずかしいです。このシステム構築が遅れているアフリカ諸国では普及が難しいかもしれません。
COVID-19へ向けたmRNAワクチンで先頭をきっている企業の一つが米製薬会社モデルナModernaです。モデルナ社はNIAIDと協力しながら人工知能AIを活用してmRNAワクチン(開発コード:mRNA-1273)を開発し、すでにマウス実験による有効性を確認しています。そして、3月16日には、mRNA-1273の初の人に対する臨床試験が開始されたことが発表されました [11, 12]。できる限り早い時期での実用化が期待されるところですが、モデルナでは1年から1年半後を見越しているようです。
治験においてはワクチンの安全性や効果はもちろんのことですが、作られたスパイクタンパク質の生体内での動態や、当該mRNAが宿主によるRNA編集を受けることなく正確に翻訳されることや、宿主ゲノムへDNAとして組み込まれないことも確かめることもきわめて重要です。原理的にmRNAはゲノムに組み込まれることはないと言われていますが、たとえば、レトロトランスポゾンは逆転写活性を有しますので、念のため調べる必要があるでしょう。
mRNAワクチンの開発については、このほか米ファイザーと独ビオンテックなど、数社が取り組んでいます。SARS-CoV-2に対するワクチンの開発をめぐっては、海外の多数の製薬会社や大学が開発にしのぎを削っており、WHOは逐次その状況を公開しています [13]。日本語のウェブ上の記事でも、その動向がアップデートされています [14]。
一方、少し出遅れているとも思える日本の状況ですが、バイオベンチャーのアンジェスが大阪大学と共同でDNAワクチンの開発に乗り出しました。技術面でのタカラバイオとダイセルの協力もあるようです [14, 15]。
DNAワクチンはさらにmRNAの手前のスパイクタンパク質遺伝子(DNA)そのものをワクチンとするものです。当該遺伝子をプラスミドに組み込みそれを運び屋として生体内に導入します。mRNAに比べれば安定性や大腸菌で大量生産できるという点において優れていますが、基本的にmRNAワクチンと同じような課題があります。
おわりに
上述したように、すでに世界中の多数の企業や機関がワクチン開発に乗り出しており、それらに期待したいところです。しかし、ワクチンが完成という見通しが立つまでにはいましばらく時間がかかります。見通しが立ったとしても実際の予防接種の段階まで行くには短くても1年半から2年の歳月はかかるでしょう。
英国BBCは「ワクチンをただ漫然と待つことを戦略という立派な名前で呼ぶべきではない。そんなものは戦略ではない」という英国エジンバラ大学のウールハウス(M. Woolhouse)教授(専門:感染症疫学)の弁を伝えました [16]。確かにそうかもしれません。
このパンデミックから脱出できる方法は具体的にはありませんが、考えられることは(1) 自然感染による集団免疫、(2) ワクチン、(3) 防疫対策とセットの恒久的な我々の行動変容、の三つです。(1)については甚大な被害を覚悟した場合であり、かつ獲得免疫が持続するという保証がない現時点では、非現実的なことは上述したとおりです。ただ、ヒトには自然免疫による感染症防御も備わっているので、集団免疫に至らないまでも(その組み合わせで)収束できる可能性もあります。
現実的には(2)と(3)でしょう。
(2)については、長期的には明らかに、ワクチンがこの危機からの脱出方法であるとウールハウス教授は述べています。できるだけ早くに開発され実用化されることを期待するものですが、一方で過大な期待は禁物です。もしワクチンの効き目が長続きしないということになれば、その活用法に工夫がいるでしょうし、上述したように現実的には免疫力の同調性を保つことが難しいので、ワクチン集団免疫によるパンデミック沈静化は不可能ではないか?(ゲームチェンジャーにはなり得ない)と個人的には考えます。あくまでもワクチンは、個人レベルでの病気の予防(発症や重症化予防)のためと考えておくべきでしょう。
(3)の私たちの行動を変えるということは、防疫対策や公衆衛生対策(非医薬的介入)とセットにした従来の経済性や利便性に基づくライフスタイルの変更です。急激な感染者の増加に鑑み、感染の拡大を抑える、封じ込めを行うために各国政府は国境封鎖、外出禁止、テレワークなどの強制的な対策を続々と出しています。
そして、恒久的に私たちの行動を変えるということは生き方の価値観を変えることにもなります。封じ込めに失敗すれば、SARS-CoV-2は変異を繰り返しながら、ワクチンの選択圧による免疫逃避によって長期間人類社会に入り込むことも想定されます。そもそも、スパイクタンパク質に特化した核酸ワクチンはその危険性(免疫逃避変異体の出現)がきわめて高いのです。そのことも前提として私たちは生き方を変えなくてはならないということです。
一方で日本はどうでしょうか。いまだに東京五輪を実施すべきかという間抜けな議論がなされていますし、テレビでは都心での人ごみを伝えています。「自分だけは大丈夫」という正常性バイアスに支配されているのでは?と思える姿があります。各国の大都市の通りのガランとした状況や人と接触しない異常な行動を観て、「信じられない」と言っている場合ではないのです。多数の感染者と死者を出すような流行の波が繰り返しやってくることに、想像を向けなければなりません。
そして国は、将来のワクチン供給と接種について計画的に進める必要があります。検査・隔離とワクチン接種は防疫対策の基本です。検査ではクラスター対策にPCR検査資源を限定投入する方針で、まったく言っていいほど防疫対策は機能していません。クラスター対策に拘泥する限り、感染拡大抑制対策は失敗するでしょう。ワクチンの供給・接種については、遅れをとるようなことがないことを望みたいものですが、厚労省の抽象的な対応は懸念材料です。この先が思いやられます。
引用文献・記事
[1] Wu, J. T. et al.: Nowcasting and forecasting the potential domestic and international spread of the 2019-nCoV outbreak originating in Wuhan, China: a modelling study. Lancet 395, 689-697 (2020).
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(20)30260-9/fulltext
[2] Kayane, S.P. et al.: New coronavirus outbreak: Framing questions for pandemic prevention. Sci. Trans. Med. 12, eabb1469. https://stm.sciencemag.org/content/12/534/eabb1469
[3] Ring, S. & Paton, J.: U.K. Says Virus Needs to Infect 60% of Britons to Save Lives. Bloomberg 13 March 2020. https://www.bloomberg.com/news/articles/2020-03-13/u-k-says-virus-needs-to-infect-60-of-britons-to-save-lives
[4] 厚生労働省:新型コロナウイルスに関するQ&A(医療機関・検査機関の方向け)https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/dengue_fever_qa_00004.html#Q16
[5] Andersen, K. G. et al.: The proximal origin of SARS-CoV-2. Nat. Med. 17 March 2020. https://www.nature.com/articles/s41591-020-0820-9
[6] Wrapp, D. et al.: Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation. Science 367, 1260-1263 (2020). https://science.sciencemag.org/content/367/6483/1260.long
[7] Wu, F. et al: A new coronavirus associated with human respiratory disease in China. Nature 579, 265–269(2020). https://doi.org/10.1038/s41586-020-2008-3
[8] Takano, T.: Antibody-dependent enhancement occurs upon re-infection with the identical serotype virus in feline infectious peritonitis virus infection. J. Vet. Med. Sci. 70, 1315–1321 (2008). https://www.jstage.jst.go.jp/article/jvms/70/12/70_12_1315/_article
[9] Wang, S.-F.: Antibody-dependent SARS coronavirus infection is mediated by antibodies against spike proteins. Biochem. Biophys. Res. Commun. 451, 208–2014 (2014). https://doi.org/10.1016/j.bbrc.2014.07.090
[10] Karikó, K. et al.: Suppression of RNA recognition by Toll-like receptors: the impact of nucleoside modification and the evolutionary origin of RNA. Immunity 23, 165-175 (2005). https://doi.org/10.1016/j.immuni.2005.06.008
[11] NIH: NIH clinical trial of investigational vaccine for COVID-19 begins. March 16 2020. https://www.niaid.nih.gov/news-events/nih-clinical-trial-investigational-vaccine-covid-19-begins
[12] 片瀬ケイ: 世界ではじめて。新型コロナに対するmRNAワクチンの臨床試験はじまる Yahooニュース 2020.03.17. https://news.yahoo.co.jp/byline/katasekei/20200317-00168217/
[13] WHO: Draft landscape of COVID-19 candidate vaccines – 20 March 2020
https://www.who.int/blueprint/priority-diseases/key-action/novel-coronavirus-landscape-ncov.pdf?ua=1
[14] 前田雄樹: 新型コロナウイルス 治療薬・ワクチンの開発動向まとめ【COVID-19】(3月19日UPDATE)AnswersNews 2020.03.19. https://answers.ten-navi.com/pharmanews/17853/
[15] 日本医事新報社: NEWS 新型コロナウイルスDNAワクチンの共同開発に着手─アンジェス・阪大. 2020.03.09. https://www.jmedj.co.jp/journal/paper/detail.php?id=14208
[16] Gallagher, J.: Coronavirus: When will the outbreak end and life get back to normal? BBC News 20 March 2020. https://www.bbc.com/news/health-51963486
引用した拙著ブログ記事
2020年3月19日 新型コロナウイルスは人為的改変体ではない
2020年3月14日 手洗いと消毒ーウイルス除去の基本
2018年5月26日 感染症と集団免疫
カテゴリー:社会・時事問題
カテゴリー:ウイルスの話
カテゴリー:感染症とCOVID-19
